作者简介:常浩生,硕士研究生,主治医师。
高位胆道梗阻一旦出现发热、黄疸、消化系统等症状, 多已失去手术机会, 或因其并发症及病死率高而放弃手术。随着介入技术的发展, 高位胆道梗阻的内支架治疗已成为重要的治疗方式[1]。高位恶性胆道梗阻的多支架技术及支架后的综合治疗, 较好地解决了胆汁的引流, 可防止肝功能进一步损害, 同时多种手段的综合运用提高了患者的生存质量。武警北京总队第二医院2014-01至2016-09综合运用多种介入技术治疗高位胆道梗阻24例, 取得良好的治疗效果。
2014-01至2016-09共收治高位胆道梗阻30例, 其中男19例, 女11例; 年龄47~76岁, 平均67.5岁。临床诊断为肝门部胆管癌11例, 原发性肝癌8 例, 结直肠癌淋巴结转移 3例, 胃癌术后肝门转移2例, 胰腺癌肝门转移 5例, 胆囊癌累及肝门1例。全部患者术前均行CT或MRI检查, 提示肝内胆管扩张, 梗阻部位位于肝门部, 经皮胆管造影证实梗阻部位位于左右胆管及肝总管汇合处。其中BismuthⅠ 型 5例, Ⅱ 型 3例, Ⅲ 型 10例(Ⅲ a 6例, Ⅲ b 4 例), Ⅳ 型12例。定性诊断依据临床表现、化验及影像学检查, 其中21例有病理学结果。本组所有患者均经肝胆外科会诊后排除外科手术可能。有6例仅单纯行右肝/左肝的PTCD, 其中放弃进一步治疗4例, 2例因肝门部肿瘤生长无法行支架置入, 共24例行介入治疗。
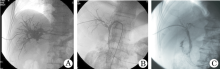
全组患者根据影像学资料, 首次治疗均采取内外引流的方式, 在内外引流3~5 d后依据患者黄疸缓解情况予以胆道支架置入或单纯行内外引流(图1A)。对于可行胆道支架的患者, 在引流管置入1周后行胆道造影, 见支架扩张良好、胆管通畅, 拔出引流管, 并根据患者肝功能及全身情况给予动脉灌注治疗。(1)抗生素治疗:术前如果疑有胆道感染, 使用适当的抗生素一次性静脉点滴或静脉推注。(2)确定穿刺路径:术前通过肝胆增强CT或MRI等影像学资料, 结合患者的原发疾病, 判断胆管梗阻的部位及受累情况。根据影像学资料初步制定治疗方案即采用单侧引流或双侧引流。患者仰卧位, 对于本组患者拟行单通道支架置入的, 在透视下选右侧第7~10肋间腋中线处穿刺右肝管。水平刺向第T11或T12右缘2 cm, 使用5 m1注射器注入稀释的造影剂, 边注入边缓慢后撤穿刺针, 直至胆道显影。胆道穿刺成功后, 选注入5~10 ml稀释的造影剂, 使肝内胆管显影, 以0.018 inch导丝置换3F套管针, 经外套管行胆管造影。根据胆管梗阻的部位程度分别选择外、内外引流, 或置入胆道内支架。对于部分拟行双侧入路的患者, 根据肝内胆管扩张情况, 在CT引导下经剑突下稍偏左侧入路穿刺左肝管。左侧肝管穿刺成功后保留0.018 inch导丝, 将患者转移至DSA下建立左侧入路。选择CT引导下穿刺是由于左肝肝实质较薄, 肝管及血管位置表浅, 盲穿可能会引起多次穿刺造成的胆道出血等损伤。同时应避免垂直穿刺, 穿刺针与左肝管长轴成60° 左右, 这样支架置入通道相对较长。(3)充分引流:通常在支架置入前先行胆道引流3~5 d待浓缩的胆汁排出及炎性水肿减轻后再将导丝送入十二指肠, 更换为内外引流。在充分引流并明确梗阻部位后, 再行内支架置入(图1B)。(4)支架置入:根据患者的影像学特征可采用T形或Y形支架置入术(图1C)。
(1)有效:黄疸迅速消退, 1周内TBIL下降1/3以上, 或2周内降至50%以上或胆管炎患者3 d体温、血象恢复正常者; (2)一般:1周内TBIL下降不足1/3, 2周内降至50%以下或胆管炎患者3 d内体温、血象波动; (3)无效:黄疸几乎不改变甚至上升, 或体温、血象显著升高。门诊及电话随访黄疸消退时间, 支架通畅时间和生存时间。支架通畅时间为支架置入至支架阻塞或患者死亡时间, 生存时间为自支架置入直至患者死亡时间。观察术后1周患者各项生化指标, 包括血清总胆红素、血清直接胆红素、血清丙氨酸转氨酶、血清谷氨酸氨基转移酶、血清碱性磷酸酶。
术后予以抗炎、保肝治疗。对于肝功能恢复较好, 黄疸消退理想的患者行肝动脉灌注化疗, 针对原发病进行治疗。支架置入后一般保留引流管1~2周, 通过造影复查支架扩张良好, 胆汁通过顺畅者拔出引流管。
采用SPSS 13.0统计软件进行数据分析, 计量资料采用
24例均成功行内外引流加胆道支架置入术, 共置入支架38枚。其中有15例给予双侧胆管同时置入支架。引流管于支架置入1周左右拔除。3例术后出现胆道感染, 3例术后出现胆道出血, 2例术后 3~4个月出现支架堵塞, 再次行PTCD或支架置入术, 平均生存6.7个月。所有支架均为裸支架, 支架长度40~80 mm, 直径6~10 mm。支架放置时其两端超过病变各1 cm。支架放置后根据其畅通情况, 决定是否用球囊扩张。支架放置完成后继续给予外引流管引流5~7 d, 根据造影情况决定是否拔出内外引流管。减黄满意率62.3%(15例), 一般8.3%(2例), 无效29.2%(7例)。术后并发胆道感染3例, 经对症处理好转。
本组随访21个月, 有2例在3~4个月发生胆道再狭窄, 再狭窄率8.3%。本组生存时间1~10个月, 中位生存时间8.7个月。生存6个月以上12例, 生存率50.0%。
高位恶性胆道梗阻患者, 发病初期一般有巩膜、皮肤黄染症状, 往往还有皮肤瘙痒和食欲缺乏、恶心、呕吐、精神状态差等其他症状, 严重影响患者生活质量和生存时间[2]。因发现时大多已失去外科手术的时机, 所以尽快、有效地减黄挽救肝功能成为当务之急。经皮经肝胆道引流是对梗阻性黄疸的一种姑息性方法。有研究表明, 姑息胆道引流治疗晚期肝门部胆管癌致梗阻性黄疸是重要选择[3]。患者血清ALT、AST、TBIL和DBIL水平在术后1周改善明显, 是不能手术切除的恶性梗阻性黄疸治疗首选方法[4], 具有操作简便、患者痛苦少、并发症少、减黄效果显著等特点。结合支架置入可迅速的恢复胆汁的肝肠循环, 同时术后予以介入栓塞可充分改善肝功能, 提高生存质量。
笔者肝门部恶性胆道梗阻支架置入体会主要有:(1)选择正确穿刺的部位, 确定单侧或双侧穿刺。对于部分特殊解剖学变异或条件无法立即实施的患者, 在CT引导下行穿刺定位, 然后再至DSA下行引流管的置入不失为一种可靠的办法。(2)穿刺针要细, 尽量减少穿刺次数。在一时无法判断穿刺针尖和胆管的关系时, 可多角度旋转造影机, 多方位判断胆管和穿刺针的关系。这一点对初学者尤为重要, 可尽量避免发生胆道出血的可能。穿刺点多选择二、三级胆管, 以便导管导丝在胆管系统操作时有较多的余地。同时穿刺针与穿刺胆管之间的角度尽量呈锐角, 以方便导丝在胆管内操作。在置入穿刺套件进入胆管向胆总管走行时, 切忌蛮力, 在胆管拐弯时尽早将钢芯拧松, 将引流管边旋转边送入, 多可将引流管越过狭窄段。否则有引起胆道出血或胆瘘的可能。(3)支架置入时, 如为多支架置入, 经两侧PTCD通道同时向胆总管置入支架, 使支架间呈Y形。支架释放时应注意两支架的位置关系, 尽量同步释放, 避免先释放的支架因完全膨胀而影响或压迫后释放支架的释放和膨胀。在使用此技术时支架置入前应多角度造影显示两侧胆管的汇合处, 确保左肝管支架的近心端位于左肝管内。采用右侧单通道支架置入时应确保支架上端尽量超过梗阻段2~3 cm, 并放置于左右肝管的汇合部。(4)在放置引流管时应保证至少有2 ~4个侧孔位于狭窄段的上方, 同时还应保证引流管孔位于肝内胆管。必要时可人工沿引流管长径螺旋形剪开引流管增加侧孔。还应注意应将引流管头端盘曲在肝总管或胆总管内。
肝门部恶性胆道梗阻支架置入并发症防治:(1)胆道出血是较严重和常见的并发症, 常因反复穿刺或置管不当所致。在选择穿刺的胆管分支应尽量是外围分支, 且长轴应与穿刺路线尽量保持最小锐角, 这样可减少门静脉损伤的可能性。本组未发生胆道出血情况。(2)胆道感染是PTCD术后常见的并发症, 可引起肝肾功能损害, 严重者并发多脏器功能衰竭。多由于胆道梗阻, 胆汁引流不畅胆道内压力升高, 病原菌滋生引起。同时引流管或支架等异物留存、胆道反复穿刺等均是其发生的原因[5]。因此, 本组在术前常规应用胆汁内浓度较高的广谱抗生素, 但仍有3例发生胆道感染。(3)支架置入后肿瘤仍在继续生长, 肿瘤组织大多通过支架的金属网眼持续浸润生长或纵向侵犯超出支架两端导致支架堵塞, 并且金属支架刺激胆管内膜过度增生, 也可导致支架堵塞[6, 7]。有50%以上术后患者可因胆泥形成等因素出现支架再狭窄, 成为黄疸复发的主要原因[8]。本组仅2例发生再狭窄。
对于合并肝内转移并不能手术切除或身体条件欠佳者, 在胆汁充分引流, 肝功能恢复的基础上可给予TACE治疗以控制肿瘤的发展。对于孤立性肿瘤并且肿瘤直径不超过4 cm的患者再联合射频消融治疗, 以尽量减少载瘤负荷。本组有9例行氟尿嘧啶+健泽+亚叶酸钙行介入化疗, 有2例行肝肿瘤射频消融+介入化疗, 中位生存期为8.7个月。本组因样本量较小, 还有待于进一步随访观察, 下一步将对综合性的治疗手段继续进行研究, 努力延长患者生命。
责任编辑 郭 青
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|