作者简介:李 胜,博士,副主任医师。
目的 系统评价红花黄色素注射液治疗脑梗死的有效性和安全性。方法 检索电子数据库搜集红花黄色素治疗脑梗死的随机对照试验,同时手工检索纳入的参考文献。经过筛选、提取资料和评估风险偏倚后,采用RevMan5.3软件对符合纳入标准的RCT进行Meta分析。结果 共纳入38个RCT,3454例患者。Meta分析结果显示:(1)红花黄色素+常规治疗组总体有效率优于各对照组(单纯常规、丹参、血栓通、川穹嗪、银杏达莫),且差异具有统计学意义( P<0.05);(2)红花黄色素对神经功能缺损评分改善程度优于对照组,差异具有统计学意义[MD=-3.14, 95% CI(-4.04,-2.24), P<0.01];(3)红花黄色素组治疗后的中医症候疗效评分平均低于对照组[MD=-3.75, 95% CI(-5.41,-2.09), P<0.01];(4)在血液流变学、出凝血功能指标、血清炎症标记物等方面,红花黄色素治疗组的改善效果同样优于对照组( P<0.05);(5)药物不良反应及毒副作用极少,安全性较高。结论 红花黄色素辅助治疗脑梗死可以有效地提高常规西药治疗效果,且安全性良好,是目前较佳的治疗方案。同时,考虑到纳入研究数量及质量的限制,上述结论尚需更多高质量并采用关键性终点指标的临床试验予以验证。
Objective To evaluate the efficacy and safety of the safflower yellow injection in the treatment of cerebral infarction.Methods Related data published by December 2015 was retrieved from PubMed, EMBASE, the Cochrane Library, VIP, CNKI, CBM and WangFang databases regarding randomized controlled tests (RCTs) about the safflower yellow injection in treating cerebral infarction. At the same time,related literature was retrieved manually. Two reviewers independently selected studies, extracted the data and assessed the risk of bias according to the inclusion and exclusion criteria. Meta-analysis of the included RCTs was performed with software RevMan5.3.Results A total of 38 RCTs involving 3454 patients were included. The results of meta analysis showed that(1)in terms of total efficiency, the safflower yellow injection combined with conventional treatment group was better than any other control group, and the difference was statistically significant ( P<0.05); (2)the safflower yellow injection could more effectively improve the National Institute of Health Stroke Scale (NIHSS)than control groups, and the difference was statistically significant [MD=-3.14, 95% CI(-4.04,-2.24), P<0.01]; (3)the average TCM syndrome score of the curative effect in the safflower yellow injection group was lower than in control groups[MD=-3.75,95% CI (-5.41,-2.09), P<0.01];(4)the safflower yellow injection was more effective than control groups in the improvement of blood rheology, blood coagulation indexes and serum inflammatory markers ( P<0.05); (5)drug adverse reactions and side effects were few.Conclusions Current evidence shows that the safflower yellow injection can improve the effect of conventional treatment of cerebral infarction,and is safe. Therefore, the safflower yellow injection combined with conventional treatment is a preferred option. Considering the quantity and quality of the included studies, clinical trials of better quality are needed.
脑梗死(cerebral infarction, CI)是神经内科临床常见病之一, 具有发病率高、致残率高、病死率高的特点[1]。随着我国人口老年化, 卒中日益成为我国人民健康的重要威胁之一[2]。研究显示:红花黄色素(safflower yellow, SY)注射液有扩张血管、调节凝血功能、减少血栓形成等作用, 在治疗脑梗死等疾病中的作用日益凸显[3, 4]。本研究采用循证医学的原理和方法, 评价SY注射液治疗脑梗死的安全性和有效性, 为临床推广应用提供参考。
1.1.1 研究类型 临床随机对照试验(randomized controlled trial, RCT)。
1.1.2 研究对象 患者年龄> 18岁, 并经头颅CT或MRI证实, 符合权威和(或)公认的脑梗死诊断标准。排除脑梗塞合并脑出血的患者。
1.1.3 干预措施 试验组:常规治疗+红花黄色素注射液; 对照组:在常规治疗基础上, 加入或不加入其他血管活性药物。
1.1.4 测量指标 (1)总有效率; (2)神经功能缺损评分(NIHSS); (3)中医症候疗效评分; (4)血液流变学; (5)出凝血功能指标; (6)血清炎性标记物; (7)不良反应及毒副作用; (8)其他。
1.1.5 排除标准 (1)试验组混杂或联合了其他血管活性药物; (2)只有摘要而缺乏全文且联系作者未回复者; (3)重要资料报告不全且联系作者未回复者; (4)同一个机构的2个研究报道了相似的随访区间及相同的目标结果时, 纳入质量更好或信息更全面的报道, 并联系第一作者澄清分歧。
本系统评价由两名评价员检索了中文/英文公开发表的随机对照试验(RCT)。计算机检索PubMed, EMBASE, the Cochrane Central Register of Controlled Trials (CENTRAL), 中国知网(CNKI), 万方数字化期刊全文数据库(WANG FANG), 维普数据库(VIP), 中国生物医学文献数据库(CBM)。检索时间均为建库至2015年12月21日。同时, 手工检索纳入文献的参考文献。如试验报告不详或资料缺乏, 通过信件与作者进行联系获取, 以尽量增加纳入文献资料。
以PubMed为例, 英文检索策略为:
#1 Safflower yellow
#2 Cerebral Infarction OR stroke OR apoplexy
#3 #1 AND #2
以CNKI为例, 中文检索策略为:
#1 红花黄色素
#2 脑梗死 OR 脑梗塞 OR 脑卒中 OR 中风
#3 #1 AND #2
由两名评价员独立完成文献筛选和资料提取, 若遇分歧, 与第三方讨论解决。提取内容主要包括纳入研究的基本资料, 干预的内容, 测量指标, 用药疗程, 病例流失率和流失的原因, 统计学方法以及风险偏倚的各项评估内容等。缺乏的资料试通过电话、传真或邮件的方式与作者联系进行补充。在涉及含有多组研究的RCT时, 提取与本文相关的试验组与对照组。
偏倚风险评估由两名独立的评价员根据Cochrane Handbook Version 5.1.0版推荐的偏倚风险评估标准[5]评估纳入的研究, 不一致的地方通过第3位评价员介入并讨论达成一致。
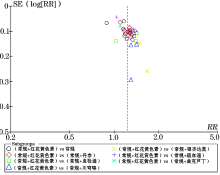
采用RevMan 5.3软件进行Meta分析[6]。首先通过χ 2检验探讨研究间异质性, 若P> 0.1, I2< 50%, 说明研究间同质性较好或异质性可接受, 直接使用固定效应模型分析; 若P≤ 0.1, I2≥ 50%, 说明研究间异质性较大, 则探讨异质性来源, 进行亚组分析和敏感性分析, 选用随机效应模型。若异质性无法解决或不适于合并, 则放弃合并分析改为描述性分析。计数资料使用相对危险度(RR)及对应的95% CI作为分析统计量; 计量资料, 则使用加权均数差(MD)及对应的95%可信区间(CI)进行分析。同时, 如果研究数量达到, 则采用漏斗图判断发表偏倚[7]。
按照以上检索策略初步检索得到相关文献489篇。使用文献管理软件去除重复文献247篇, 经过阅读全文, 进一步剔除不符合纳入标准的文献, 最终纳入38篇RCT[8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45], 共3454例受试者。纳入研究基本特征(表1)。
| 表1 红花黄色素注射液治疗脑梗死纳入研究资料的基本特征 |
根据Cochrane协助网推荐的偏倚风险评估方法, 纳入的38个研究基线具有可比性, 但均有不同水平的偏倚。38个研究[8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45]均提及“ 随机” , 其中一个描述为计算机随机[40], 一个描述按就诊顺序随机(假随机)[12]。分配隐藏方面, 一个研究提及信封法[30]。所有研究[8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45]均未报道是否评价者盲法。分别有两个研究在结果数据完整性[16, 40]、选择性报道[37, 42]方面存在高风险, 其中一个研究[40]还具有低风险的其他偏倚。
2.3.1 总有效率 31个研究[8, 9, 10, 11, 12, 13, 14, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 28, 29, 30, 31, 34, 35, 36, 37, 38, 41, 42, 43, 44, 45]均报告了总有效率, 纳入各研究间存在中度异质性(P=0.001, I2=50%), 用随机效应模型合并分析。合并结果显示:试验组对脑梗死的总体改善率优于对照组[RR=1.22, 95%CI(1.16, 1.29), P< 0.01]。探讨异质性来源可能为对照组所使用的药物不同所致, 故采用不同对照药物进行亚组分析(图1)。
2.3.2 神经功能缺损评分 23个研究[8, 11, 12, 14, 16, 18, 19, 20, 21, 22, 23, 26, 27, 30, 32, 33, 34, 37, 38, 39, 41, 43, 44]报告了治疗后神经功能缺损评分的结果, 且均描述了两组治疗前NIHSS评分无统计学差异(P< 0.05)。纳入文献中各研究间异质性较大(P< 0.001, I2=94%), 使用随机效应模型合并分析。结果显示:试验组评分优于对照组[MD=-3.14, 95%CI(-4.04, -2.24), P< 0.01](图2)。敏感性分析发现依次分别剔除各项研究, 合并效应量仍都具有统计学意义且森林图结构均未发生改变。
2.3.3 其他检测及疗效指标 已纳入的研究对治疗后其他几项检查指标水平进行比较, 合并后分析结果如表2。合并分析发现治疗后血浆ET-1、血清MDA水平显著升高, 血清SOD、ADL评分显著下降; 固定效应模型合并分析同质性较好(P=0.52, I2=0%)的两个研究, 结果SY组中医症候疗效评分优于对照组[8, 32]; 两个研究合并结果显示SY组患者治疗后的血清IL-1β 、TNF-α 水平下降比对照组更低[33, 40]; 还有研究显示患者血清IL-6、凝血象相关指标, 以及NT-proBNP在治疗前后明显改善[40, 43]。11项研究描述治疗前两组血液流变学指标差异无统计学意义(P> 0.05); 治疗后较治疗前两组均明显改善, 其中干预组优于对照组(P< 0.05)[8, 9, 10, 12, 22, 23, 32, 35, 37, 40, 42]。
| 表2 红花黄色素注射液治疗脑梗死治疗后其他检测指标比较的Meta分析 |
2.3.4 不良反应及毒副作用 25个研究描述了药物不良反应及毒副作用的情况[8, 9, 10, 11, 13, 14, 15, 16, 18, 21, 24, 25, 26, 28, 29, 30, 31, 32, 35, 36, 38, 39, 40, 42, 44], 其中有18个研究在治疗过程中均未发生明显不良反应[8, 9, 10, 13, 14, 15, 18, 21, 25, 26, 29, 30, 31, 32, 35, 36, 38, 42]。柳学勇和郑佳英[11]的研究提及试验组有2例患者轻度发热, 但未影响研究的进行。耿昌等[16]研究报道治疗组有1例患者治疗时出现皮疹, 退出试验。金虹艳等[24]研究报道:SY治疗组中有1例患者出现了发热、轻度嗜睡的症状, 有1例出现了皮肤过敏性丘疹, 停药后恢复; 丹参治疗组2例出现了发热的症状, 3例出现了皮肤过敏性丘疹, 1例出现了过敏性休克的症状。韩英等[28]的研究指出:治疗组3例患者可能因上呼吸道感染而出现治疗后白细胞升高。武桂花[39]的研究中, 血栓通组1例患者出现轻微皮疹。宁丽洁[44]和Li等 [40]两位研究者都描述:SY组有2例轻微发热, 对症处理后迅速缓解与对照组相比差异无统计学意义。
本研究对38个使用SY注射液治疗脑梗死的RCT进行了系统评价和Meta分析。经分析, 在总有效率、神经功能缺损评分方面, SY辅助治疗脑梗死可以更有效地提高常规西药治疗效果, 其中仅一篇文献表述SY优于疏血通但无统计学意义; 在中医症候疗效评分方面SY组治疗后疗效评分平均低于对照组; 多个研究采用不同指标描述了血液流变学指标、凝血功能、以及其他检测指标在治疗后有改善, 且SY组改善优于其他各对照组; 安全性比较中SY组较好。
本研究的局限性:(1)纳入研究的方法学质量偏低, 缺乏足够的信息判断临床试验的合理性, 如随机、分配隐藏、盲法等; (2)部分结局指标纳入研究数量有限, 未能合并分析。如:凝血功能指标等, 只能采取描述性分析; (3)纳入研究均未采用终点指标作为观察对象(如心脑血管事件发生率、死亡率); (4)虽然采用了广泛的检索策略, 但诸如会议论文、部分灰色文献无法获取, 且纳入研究信息的限制, 该研究只能就相关指标予以合并分析或评价, 因而不能排除发表偏倚的可能[46]; (5)本研究检索虽未限制语种, 但经检索后仅纳入1篇英文文献, 可能影响研究结果的外推性。此外, 一些研究样本量的限制以及研究设计的局限, 使得对研究结果的可靠性尚需大样本、高质量的研究予以证实。
综上所述, 当前证据表明, SY辅助常规西药治疗脑梗死安全有效, 可明显改善神经功能缺损、血液流变学和凝血功能指标等, 是目前最佳的治疗方案之一, 推荐临床医师合理采用。同时, 考虑到纳入研究数量及质量的限制, 建议今后严格按照CONSORT标准[7]设计出高质量、大样本、多中心的研究并采用关键性终点指标, 对本研究结果进一步验证。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|