作者简介:杨洋,硕士研究生,医师。
目的 采用Meta分析系统评价18F-FDG PET/CT对非小细胞肺癌EGFR基因突变的诊断价值。方法 计算机检索PubMed、EMbase、The Cochrane Library、中国期刊全文数据库、万方数据库、中文科技期刊数据库,查找有关18F-FDG PET/CT对非小细胞肺癌EGFR基因突变的诊断性试验。由 2 位评价员按照纳入与排除标准独立筛选文献、提取资料和评价纳入研究的方法学质量后,采用Meta DiSc1.4软件进行Meta分析。结果 最终纳入16篇文献,非小细胞肺癌3308例。病理确诊为肺腺癌2914例(88.09%),其他病理类型394例(11.91%)。Meta分析结果示,SEN合并=0.57[95% CI(0.55,0.60)],SPE合并=0.65[95% CI(0.62,0.67)],+LR合并=1.82[95% CI(1.49,2.23)],-LR合并=0.67[95% CI(0.59,0.76)],DOR合并=2.93[95% CI(2.08,4.15)],AUC=0.6678。结论18F-FDG PET/CT的SUVmax对NSCLC患者的EGFR突变有一定的预测能力,其特异度优于敏感度,可以用于EGFR突变的诊断。
Objective To evaluate the diagnostic value of18F-FDG PET/CT for EGFR gene mutation in non-small cell lung cancer with Meta analysis.Methods Databases that had been searched included PubMed, EMbase, the Cochrane Library, Chinese Journal Full-text Database, Wanfang Database, Chinese Science and Technology Database. Diagnostic tests related to EGFR gene mutation in non-small cell lung cancer and involving18F-FDG PET/CT were investigated and analyzed. Meta-analysis was performed using Meta DiSc 1.4 software after two reviewers independently screened the literature for inclusion and exclusion criteria, extracted the data and evaluated the methodological quality of the included studies.Results 16 articles and 3308 cases of non-small cell lung cancer patients were included. Meta-analysis results showed that the incorporated SEN averaged 0.57[95% CI (0.55,0.60)], incorporated SPE 0.65[95% CI (0.62,0.67) CI (1.49,2.23)], incorporated LR 0.67[95% CI (0.59,0.76)], and incorporated DOR 2.93[95% CI (2.08,4.15)], while AUC was 0.6678.Conclusions SUVmax of18F-FDG PET/CT is of predictive value for the mutation of EGFR in NSCLC patients with better specificity than sensitivity, which can be used to predict the mutation of EGFR in NSCLC patients.
非小细胞肺癌(non-small cell lung cancer, NSCLC)占肺癌的80%~85%[1]。在原发性NSCLC中, 肺腺癌是最常见的组织学类型, 预后很差[2]。近年来, 靶向药物表皮生长因子受体(epidermal growth factor receptor, EGFR)酪氨酸激酶抑制药(TKIs)在NSCLC治疗中得到很好的应用。EGFR在NSCLC中存在突变和野生两种类型[3], 而EGFR-TKIs明显延长EGFR突变型的无进展生存期(PFS)[4]。因此, 对EGFR突变进行有效预测可以指导临床治疗, 评估预后。现有研究表明, 氟18氟代脱氧葡萄糖(18-fluoro-2-deoxyglucose, 18F-FDG) PET/CT利用肿瘤组织与周围正常组织的代谢差异, 可以对EGFR突变有预测作用[5]。但对EGFR突变预测最大标准化摄取值(max standardized uptake value, SUVmax)的取值大小有所争论[6, 7, 8, 9, 10, 11, 12, 13] 。本研究检索截至2017-12关于18F-FDG PET/CT对NSCLC患者EGFR突变的相关文献, 对其诊断价值进行Meta分析, 为临床决策提供参考。
纳入标准:(1)文献类型为18F-FDG PET/CT对NSCLC EGFR基因突变的诊断文献; (2)研究类型为诊断性研究, 主题为利用PET/CT检查获得NSCLC患者的SUVmax值; (3)研究对象均为经病理学诊断明确为肺腺癌的患者, 所有患者均经18F-FDG PET/CT检查; (4)诊断均对组织标本进行 EGFR 基因突变检测。(5)结局指标敏感性(SEN)、特异性(SPE)、阳性似然比(+LR)、阴性似然比(-LR)、诊断比值比(DOR)、受试者工作特征曲线(SROC 曲线)下面积(AUC)。
排除标准:(1)18F-FDG PET/CT检查EGFR基因没有SUVmax等代谢参数的数据的文献; (2)会议、病例报道、动物实验、评论、综述性文献和基础研究文献; (3)病例数少于10例的文献; (4)数据不全、错误、或数据不清晰的文献; (5)重复发表的文献。
1.2.1 数据库 文献检索的英文数据库包括PubMed、EMbase、The Cochrane Library; 中文数据库包括中国期刊全文数据库、万方数据库、中文科技期刊数据库。各个数据库的检索年限均为从建库至2017年12月。
1.2.2 检索词 Flurodeoxygluose F18、FDG、18F-FDG、non-small cell lung cancer、NSCLC、adenocarcinoma of the lung、Lung adenocarcinoma、EGFR、Receptor、Epidermal Growth Factor。中文检索词:正电子发射计算机体层摄影、非小细胞肺癌、肺腺癌、18F-氟脱氧葡萄糖、表皮生长因子受体。
分别由 2 名研究员独立按上述标准进行文献筛选, 集体讨论或由第三方裁决所遇分歧。提取数据包括以下内容:作者, 发表时间, 研究国家, 患者数量, 患者性别, PET扫描仪型号, 纳入患者的组织病理学TNM分期, 临界值及实验方法。将最终纳入文献的灵敏性、特异性、真阳性(TP) 、假阳性(FP) 、真阴性(TN)、假阴性(FN)提取至四格表。
分别由2名评价者采用诊断性研究质量评价量表(quality assessment of diagnostic accuracy studies, QUADAS) 中的14个条目对所纳入文献进行质量评价, 评价内容包括3个方面(变异、偏倚、报告质量), 存在异议的条目通过讨论达成共识。每个条目标准按“ 是” (满足条件)、“ 否” (不满足或未提及)或“ 不清楚” (部分满足或无法从文献中得到足够信息)3个评价等级, 找出偏倚与变异产生的原因。
使用Meta-Disc 1.4统计软件进行Meta分析。通过χ 2检验进行异质性分析, 使用Cochrane Q检验和I2评估异质性[14]。 P< 0.05表示显著异质性。I2值为0%表示无异质性, 小于25%表示低异质性, 25.1%~50%表示中等异质性, 而大于50%表明有非常大的异质性。当观察到无、低或中等异质性时, 使用固定效应模型来计算汇集的HR。
根据检索词共检索595篇相关文献, 其中中文文献344篇, 英文文献251篇。利用Endnote软件删除重复文献88篇, 最终纳入文献16篇。
共涉及NSCLC患者3308例, 其中男1918例(57.98%), 女1390例(42.02%), 中位数年龄为62.5岁, 病理确诊为肺腺癌2914例(88.09%), 其他病理类型394例(11.91%)(表1、2)。
| 表1 非小细胞肺癌研究纳入Meta研究的基本特征 |
根据本研究特点, 将QUADAS中的10、12条目删除。所有纳入文献的金标准均为经过EGFR检测的病例, 且检测方法为自动仪器化结果, 金标准的检测方法不存在偏倚。对纳入文献的研究方法学进行质量评价, 其中“ 1” 代表低度偏倚或适用性好; “ -1” 代表高度偏倚或适用性差; “ 0” 代表缺乏相关信息或偏倚情况不确定。为避免评价偏差, 由 2 名评价者独立进行评估且交叉核对, 共同讨论意见分歧或由第三方判决。
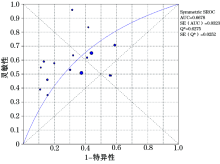
SROC曲线不呈典型“ 肩臂状” 分布, 显示不存在阈值效应。由于SPE合并、SEN合并、+LR合并、-LR合并和DOR合并显示在非阈值效应引起的异质性, 所以此Meta分析采用随机效应模型(图1)。
Meta分析结果示, SEN合并=0.57[95%CI(0.55, 0.60)], SPE合并=0.65[95%CI(0.62, 0.67)], +LR合并=1.82[95%CI(1.49, 2.23), -LR合并=0.67[95%CI(0.59, 0.76)], DOR合并=2.93[95%CI(2.08, 4.15)], AUC=0.6678。
肺癌是最常见的癌症之一, 是全球癌症相关死亡的主要原因。NSCLC是肺癌中最常见的病理类型。EGFR-TKIs已被美国临床肿瘤学会(ASCO), 欧洲肿瘤内科学会(ESMO)和美国国家综合癌症网络(NCCN)推荐为EGFR突变阳性的NSCLC晚期患者的一线治疗药物。中国NSCLC治疗指南提示, 在非小细胞肺癌的靶向药物TKI治疗前需要EGFR基因检测的支持[28], 但临床中经常出现难以穿刺获得病理或者获得的病理组织不够的情况, 增加了治疗的困难。Yip等[29]将FDG PET/CT的放射学特征和NSCLC肿瘤细胞表型相关联, 发现SUVmax、MTV(Metabolic Tumor Volume, 肿瘤代谢体积)、TLG(Total lesion glycolysis, 肿瘤糖代谢总量)等指标对NSCLC的EGFR突变有预测作用。并且FDG PET/CT作为非侵入检查方式更易被患者接受。
笔者将SUVmax对NSCLC患者的EGFR突变的预测效能进行了系统评价。首先SUVmax的数据获得十分方便, 并且PET/CT对SUVmax的测量差异较小; 其次很多研究者对NSCLC患者的代谢参数MTV的测量标准不一, 定义MTV使用不同的标准, 如SUV2.5, SUV3.0和SUV40%, 存在异质性从而无法进行系统评价; 最后由于TLG的测量方法为SUVmax与MTV的乘积, 所以同样存在较大的异质性。
有研究得出FDG PET/CT的代谢参数对NSCLC患者的EGFR突变有预测作用, 但研究结果各不相同, 分析其结果出现差异的原因, 可能是样本量较少, 研究对象的年龄、种族等差异。本系统评价制定了较完善的检索策略, 检索了多个中外主要数据库, 最终纳入16篇中外文献, 进行数据提取及分析, 共计3308例NSCLC患者, 其中肺腺癌2923例, 目的是降低因样本量少和选择偏倚而出现的结果误差。合并分析表明, SUVmax对NSCLC患者EGFR基因突变的诊断平均敏感度57%, 平均特异度为65%, 表明其误诊率为35%, 漏诊率为43%。平均阳性似然比1.82, 平均阴性似然比0.67, 表明SUVmax对EGFR突变状态有统计学意义的预测作用, 但是测量所得SUVmax的取值范围在EGFR突变组和野生型组之间存在重叠。AUC为0.6678, 表明SUVmax具有一定的诊断效能。
本研究存在的问题及不足:(1)纳入的文献中多数未将人种因素作为分组, 而进行分析, 文献多数来自亚洲, 这样对纳入人群的选择存在一定的选择偏倚。(2)各个文献中进行PET/CT扫描的机型不同, 并且18F-FDG的注射的剂量及检查所用时间均有差异, 使结果存在一定的测量偏倚。(3)文献的检索范围均来源于已发表的国内外主流数据库, 对一些未发表的文献未进行纳入, 可能存在漏检。
总之18F-FDG PET/CT的SUVmax对NSCLC患者EGFR的突变有一定的预测能力, 对临床中EGFR突变的诊断具有价值。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|