目的 评价负压创面疗法 (negative pressure wound therapy, NPWT)治疗猪铜绿假单胞菌感染创面的效果。方法 取巴马香猪24只,随机分为NPWT组(负压组)和无菌纱布治疗组(对照组),每组12只,在背部建立一个直径5 cm的铜绿假单胞菌感染创面并分别采用相应治疗方法。于建模成功后及治疗的第4、8、12、16天取材进行细菌计数及细菌侵袭深度分析,取1 g创面敷料用于eDNA(Extracellular DNA)分析。结果 开始治疗后负压组创面细菌计数小于对照组,从治疗的第8天开始差异有统计学意义( P<0.05),之后均明显低于对照组,在治疗的第16天时两组细菌计数分别为(1.92±0.79)和(3.50±0.80),以对数lg值表示( P<0.001);生物膜成分eDNA检测显示在治疗的第4、8、12、16天时负压组明显低于对照组( P<0.05)。随着治疗时间的延长,两组创面细菌平均侵袭深度均逐渐减少。但负压组细菌侵袭深度在治疗后的取材时间点上均明显低于对照组( P<0.05),治疗的第16天时细菌侵袭深度分别为(18.2±9.7)μm和(40.0±12.3)μm,差异有统计学意义( P<0.01)。结论 与对照组相比,负压组可降低铜绿假单胞菌感染创面细菌计数,减少创面eDNA成分,降低细菌侵袭深度。这可能是NPWT减轻感染机制之一。
Objective To quantitatively analyze the clinical effect of negative pressure wound therapy on Pseudomonas aeruginosa infected wound in a porcine model.Methods Twenty-four Bama miniature pigs were included in this study. All these animals had a wound 5 cm in diameter created on the back and infected with Pseudomonas aeruginosa before they were randomly divided into two groups: negative pressure wound therapy group (NPWT) and sterile gauze treatment group. After the infected model was established, samples were collected for analysis of bacterial count and bacterial invasion depth on day 0, 4, 8, 12 and day16. Wound dressing (weight, 1 g) was also collected for eDNA analysis.Results After treatment, the bacterial count in the NPWT group was lower than that of the control group and the difference was statistically significant from the 8th day ( P<0.05). The bacterial counts in the NPWT group and the control group were 1.92±0.79 and 3.50±0.80 respectively(expressed as the logarithm, P<0.001) on the 16th day. The results of eDNA showed that the bacterial count of the NPWT group was significantly lower than that of the control group on the 4th, 8th, 12th and 16th days ( P<0.05). With the extension of treatment, the average invasion depth of the two groups was gradually decreased. However, the bacterial invasion depth of the NPWT group was significantly lower than that of the control group on the 4th, 8th, 12th and 16th days ( P<0.05). Bacterial invasion depth in the NPWT group and the control group was (18.2±9.7)μm and (40.0±12.3)μm ( P<0.01)respectively.Conclusions Compared with conventional gauze treatment group, negative pressure wound therapy can significantly reduce the bacterial count, eDNA amount and invasion depth for Pseudomonas aeruginosa infected wound. This may be one of the mechanisms by which negative pressure wound therapy can promote wound healing.
创面污染能否导致感染形成常取决于致病菌的类型和数量, 一般创面软组织内细菌数量达到105 CFU/g (tissue)即可认为达到临床感染标准[1, 2]。因此, 减少或杀灭软组织内的细菌是治疗软组组感染的重要目标, 也是用来衡量软组织感染治疗状况的重要指标之一。负压创面疗法 (negative pressure wound therapy, NPWT)在严重开放性骨折创面、糖尿病足溃疡、下肢静脉溃疡等治疗方面已经得到广泛应用 [3, 4, 5, 6, 7]。近年来, 众多研究相继报道NPWT在感染性创面的应用, 发现其可以减轻创面感染程度, 加速创面愈合 [8, 9, 10, 11]。然而, 目前报道NPWT治疗下铜绿假单胞菌感染创面生物膜变化、生物膜成分改变, 以及细菌在软组织内的侵袭深度的研究较少。
巴马香猪24只, 术前适应性饲养1周。经过麻醉、脱毛及消毒, 在巴马香猪背部建立一个直径5 cm深达肌肉层的软组织创面, 去除肌肉腱膜, 充分止血后接种0.5 ml表达绿色荧光蛋白的铜绿假单胞菌菌液(总菌量为5× 107 CFU), 涂抹均匀, 半透明膜敷料覆盖24 h, 以确保细菌的稳定黏附和定植。本研究经过我院动物伦理委员会审查。
半透明膜敷料覆盖24 h后(建模成功)将巴马香猪随机分为NPWT组(负压组)和无菌纱布治疗组(对照组), 每组12只, 分别进行治疗。密切观察敷料变化情况, 每两天更换敷料1次。分别于治疗的第4、8、12、16天取材。
将标本称重并记录。首先用无菌组织剪充分剪碎组织标本, 按照组织标本与无菌PBS缓冲液的重量比为1∶ 99的比例混合, 于研磨器中再次充分研磨。依照倍比稀释法按浓度梯度稀释, 最后分别吸取100 μ l稀释液均匀涂抹于LB固体培养液, 37 ℃培养24 h后计数。选取LB固体培养液细菌计数在30~300个作为统计数据, 每一个浓度梯度涂抹重复3次, 取平均值, 最终软组织内细菌计数单位为CFU/g tissue。
取创面敷料1 g, 置于离心管中, 加入无菌1 ml PBS缓冲液, 涡旋震荡3 min, 充分洗脱敷料上的细菌及生物膜 [12, 13]。4 ℃, 13 400 g条件下高速离心, 去除不溶性物质, 取100 μ l上清液, 用微量样品DNA提取试剂盒抽提其中的eDNA, 具体提取过程依据试剂说明书。采用Qubit® 2.0核酸蛋白定量仪测定DNA浓度, 最终每个创面eDNA浓度单位为μ g/ml。
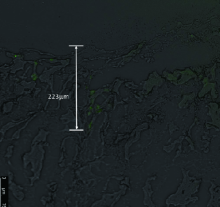
取巴马香猪肌肉组织标本。冷冻切片机内切取标本, 注意标记标本的创面一侧。激光共聚焦显微镜观察, 使用自带软件测量细菌从表面侵袭至最深处的深度并记录。每组随机选取6张, 取每一张切片内细菌侵袭深度最深的值作为统计数据。图形制作软件采用Graphpad prism 5.0。
采用SPSS 22.0统计软件, 细菌计数、eDNA含量、细菌侵袭深度等计量资料采用
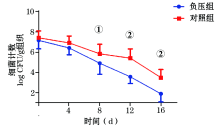
模型建立成功, 负压组和对照组细菌计数均在107 CFU/g tissue左右。在治疗后的第8天负压组软组织内细菌计数明显低于对照组, 差异有统计学意义, 其中负压组细菌计数达临床感染标准105 CFU/g 组织左右, 而在治疗的第16天两组细菌计数均低于临床感染标准, 分别为10~104 CFU/g组织和102~105 CFU/g组织(图1)。
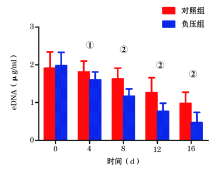
治疗后第4天创面生物膜成分eDNA定量检测显示负压组与对照组含量分别为(1.61± 0.20)μ g /ml和(1.82± 0.28)μ g /ml, 差异开始有统计学意义(P< 0.01), 在治疗的第8、12、16天负压组eDNA水平均明显低于对照组(P< 0.01, 图2)。
创面软组织内细菌数量一定程度上决定了感染的程度。早前研究多数致力于探讨NPWT治疗下创面细菌数量的变化, 然而未见研究报道NPWT可以将创面软组织内细菌降至临床感染标准以下(105 CFU/g), 这可能与观察时间不够长有关, 因为早前研究多数观察至治疗后1周左右[14, 15]。本研究采用巴马香猪软组织感染模型对NPWT进行探索, 并观察至治疗的第16天。在观察至第12天时实验组细菌计数已低于临床感染标准, 在观察至第16天时两组细菌计数均低于临床感染标准, 但此时实验组细菌计数已达103 CFU/g tissue以下。而创面细菌数量的降低的原因可能是以下两方面, 首先是NPWT的持续引流作用, 其次是创面eDNA的减少致使细菌失去了一定的保护作用。早前研究报道eDNA是细菌生物膜的重要组成部分[16, 17, 18], 而eDNA成分也能够支持铜绿假单胞菌的黏附作用[19, 20]。而本研究中生物膜的关键成分eDNA定量检测显示实验组在治疗后创面eDNA的浓度明显低于对照组, 这说明NPWT可以在治疗早期降低创面铜绿假单胞菌生物膜的关键成分。
细菌在软组织内侵袭的深度决定了感染的深度, 也决定了细菌在创面的哪一个层面定植、增殖。目前, 未见报道负压环境下创面细菌侵袭深度的相关研究。本研究采用激光共聚焦显微镜观察细菌侵袭深度, 结果显示NPWT治疗下铜绿假单胞菌软组织内侵袭深度明显低于对照组, 这可能有两方面原因, 第一是得益于NPWT的负压作用, 在负压的作用下海绵与创面软组织贴附紧密并且不断吸引, 而此时的软组织如果是在海绵的孔内则受到负压引流作用, 如果是与海绵贴附那么软组织则受到压力作用, 无论是压力作用还是引流作用可能都不利于细菌的进一步深度侵袭; 第二可能是NPWT可以减少生物膜重要成分eDNA, 阻碍细菌在创面的稳定黏附和定植, 在这种情况下, 同时感染所致的坏死物质会被及时引流, 创面上缺少了保护细菌的污物, 此时细菌可能直接面对创面组织细胞和免疫细胞, 这可能会加大机体免疫对细菌的清除作用, 也避免了细菌对创面的进一步深度侵袭。而常规纱布治疗组随着治疗时间的延长细菌侵袭深度也逐渐减小, 但其深度均高于负压组, 这也与在治疗期间发现对照组创面坏死物质较多相一致。
本研究的不足是仅采用单一细菌做感染模型, 而临床中创面感染多为多重细菌的混合性感染; 本研究采取野生型铜绿假单胞菌细菌作为感染菌株, 对抗生素较为敏感, 临床感染菌株常为耐药性, 而本研究未对耐药性菌株进行探索。
综上所述, NPWT治疗铜绿假单胞菌感染性软组织创面可以清除创面生物膜的重要成分, 减少创面细菌数量, 尤其是在治疗的中后期可以将创面细菌降至临床感染标准以下, 这一速度明显比常规的无菌纱布治疗方法快。本研究为NPWT治疗感染性软组织创面提供了理论基础。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|